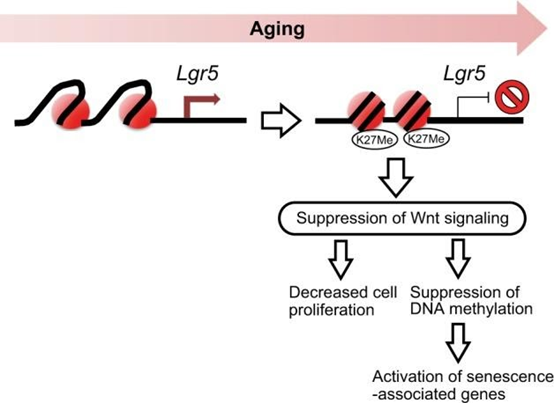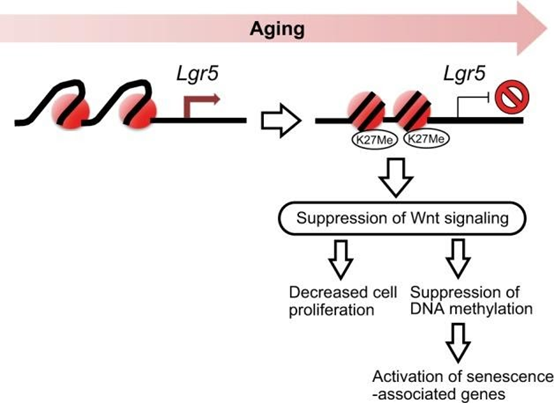
加齢に伴い、DNAの分子変化によりLgr5遺伝子の活性が低下する。このLgr5遺伝子は、細胞増殖の低下と加齢に伴う遺伝子の活性化につながる。
BW
幹細胞が自己再生して成熟細胞に分化する能力は、組織の維持と損傷の治癒に重要である。幹細胞は人の一生で体内に留まるため、細胞の損傷を受けやすくなり、最後に細胞死と組織の再生能力の喪失が生じる。このプロセスは「幹細胞の老化」と呼ばれている。
幹細胞の老化を制御することによって、健康寿命を最大限に延ばすための介入が可能になるかもしれない。そのためには、科学者は幹細胞の生存、自己再生、および増殖に関わる細胞プロセスを理解する必要がある。
日本の慶應義塾大学の研究者らは、老化した腸の幹細胞においてLgr5という遺伝子の活性が低下すると、細胞増殖が低くなる一方、老化関連遺伝子が活性化になることを発見した。ニコチンアミド・モノヌクレオチド(NMN)を投与した後、これらの加齢に伴う細胞への影響が改善された。
腸内には「絨毛」と呼ばれる細胞からなる突起部があり、顕微鏡で見ると指のように見える。これらの指のような突起部の間には、腸の幹細胞を宿す「陰窩」(crypt)と呼ばれる谷がある。若い腸内と古い腸内を比較すると、老齢マウスでは絨毛と陰窩が少ないことがわかった。このような結果から見れば、歳を重ねて細胞増殖が低下するというのは絨毛と陰窩が形成するために細胞増殖を必要とするからだということが示された。
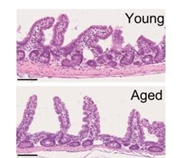
高齢マウスでは、腸内で細胞の陰窩(細胞の突起部の区域)の数が減少した。
遺伝子活性解析を行ったところ、細胞増殖の低下はLgr5遺伝子の活性低下によるものであることが判明した。Lgr5は、細胞増殖のメカニズムに関与するタンパク質をエンコードする。Lgr5遺伝子の活性が低下すると細胞増殖が低下する。その故、老齢マウスにおける腸の陰窩と絨毛の数が少なくなることが説明できる。
老化した腸の幹細胞群(オルガノイドとも呼ばれる)へのNMN治療により、細胞増殖が増加した。NMNは、これらの細胞のNAD +レベル及びSIRT1の活性を増加させた。SIRT1とは、DNA及びタンパク質上の分子タグを除去・付加することで細胞の健康を維持するタンパク質である。これらの結果から、NMNで細胞のNAD +レベルを増加させることで、マウスにおける腸幹細胞の細胞増殖を改善できる可能性が示唆された。
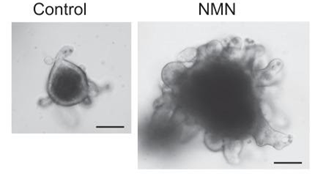
オルガノイドとも呼ばれる腸の幹細胞群をNMNで治療すると、細胞増殖が増加した。
研究者らは、高齢動物から抽出したオルガノイドが幹細胞老衰の研究および抗老化治療法の開発において強力な研究ツールになるでしょうと指摘した。
「今後の研究では、これまでに得られた結果を検証するために、ヒト細胞を用いた実験が必要になる。またその更なる研究は、健康寿命を延ばすための治療にもつながる可能性がある。」と述べた科学者らは、今後の研究でヒト細胞を使用することに言及した。
出典
情報源:
Uchida R, Saito Y, Nogami K, et al. Epigenetic silencing of Lgr5 induces senescence of intestinal epithelial organoids during the process of aging [published correction appears in NPJ Aging Mech Dis. 2019 Mar 7;5:5]. NPJ Aging Mech Dis. 2018;5:1. Published 2018 Dec 1. doi:10.1038/s41514-018-0031-5.
参照論文:
Oh J, Lee YD, Wagers AJ. Stem cell aging: mechanisms, regulators and therapeutic opportunities. Nat Med. 2014;20(8):870-880. doi:10.1038/nm.3651.